
TRABAJOS CIENTIFICOS
Plantas medicinales, aromáticas y tintóreas.
 |
|
||
Anales de SAIPA - Sociedad Argentina para la Investigación de Productos Aromáticos
IX CONGRESO NACIONAL DE RECURSOS NATURALES AROMÁTICOS Y MEDICINALES
Volumen XVI - 2000 - pág 125 a 129.
RESUMEN
La composición química del aceite esencial de las partes aéreas de Artemisia douglassiana Bess. se estudió por cromatografía gaseosa capilar y por GC/MS.
Aproximadamente el 15% del aceite esencial está compuesto por a-tuyona (67.6%) y |3-tuyona(7.6%).
The chemical composition of the essential oil obtained from the aerial parís Artemisia douglassiana Bess. was investigated hy capillary GC and GC/MS
Approximately 75 % ofthc essential oil iscomprisedof a-thujone (67.6%) and (�-thujone (7.6%).
INTRODUCCIÓN
Artemisia douglassiana Bess. conocida vulgarmente como "matico", es utilizada en la medicina popular por sus propiedades antiulcerosas, tanto por la vía interna como en forma externa. Es una Asteráceae rizomatosa y aromática que crece en la región de Cuyo (Argentina), y cuyos caracteres morfoanatómicos han sido descriptos por Ariza Espinar y col. (1)
Existen trabajos previos sobre el estudio de la composición química de esta especie, obtenida de diferentes regiones, que demuestran que posee una amplia gama de compuestos, variando éstos según el estado de maduración y la estación del año.(2,3.4.5.6) De las partes aéreas de esta especie se ha aislado una lactona sesquiterpénica, dihidroleucodina (7). con actividad citoprotectora gástrica (8). lo que convalida su uso popular como antiulcerosa.
Los aceites esenciales del género Artemisia han sido siempre de interés para químicos v taxonomistas debido u la importancia medicinal e industrial y por la composición química heterogénea de algunas variedades y quimiotipos. (9,10)
Se ha descripto la variación ontogenética y diurna de 33 componentes del aceite esencial de A. douglassiana recogida en la región de California, USA. (11)
OBJETIVOS
El objetivo del presente trabajo es la identificación de los componentes del aceite esencial de las partes aéreas de Artemisia douglassiana Bess. proveniente del norte de la provincia de San Luis.
MATERIALES Y MÉTODOS
El material vegetal fue recolectado en la Estancia Piedra Blanca, de la localidad de Lujan en la serranía del Comechingones, provincia de San Luis y clasificado por la Dra. Marta Nájera de la Universidad Nacional de La Plata (LPE 927).
El aceite esencial se obtuvo a partir de las hojas secas por hidrodestilación en una trampa tipo Clevenger de acuerdo al método descripto en la Farmacopea Francesa X Ed. con un rendimiento de 0.6 %.
La identificación de los componentes del aceite esencial se realizó por:
Determinación de los índices de retención (IR) relativos a una serie homóloga de ésteres metílicos de ácidos grasos (C4-C18) en dos columnas de diferente polaridad: Carbowax 20M (CW20-M) y Metilsilicona SE-30 (SE-30), utilizando un Cromatógrafo de gases Varían Star 3400 equipado con un detector de ionización de llama y columnas capilares con las fases estacionarias antes mencionadas (60 m x 0,25 mm). Las condiciones analíticas fueron las siguientes: Detector (255�C), inyector (255�C), split 1/95, temperatura isotérmica 4 min. a 75�C, temperatura programada de 75�C a 220�C (3�C/min.) y temperatura isotérmica 15 min. a 220�C, utilizando nitrógeno como gas carrier (0,9 ml/min.).
La cuantificación de cada componente se determinó a partir de los valores de áreas relativas bajo estas mismas condiciones en ambas columnas.
CG/MS en CW20M y SE-30. Comparación con espectros citados en bibliografía (12,13,14). Este análisis se llevó a cabo utilizando un Cromatógrafo de gases acoplado a un espectrómetro de masa Perkin Elmer Q-Mass 910 y columnas capilares con las fases estacionarias antes mencionadas (30m x 0,25 mm). Condiciones analíticas: inyector (250�C), split 1/100, temperatura programada de 75�C a 220�C (4�C/min), temperatura isotérmica 5 min. a 220�C, voltaje de multiplicador (HV): 1150, utilizando helio como gas carrier (1 ml/min).
RESULTADOS Y DISCUSIÓN
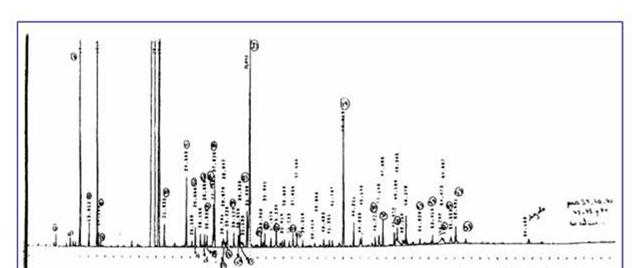
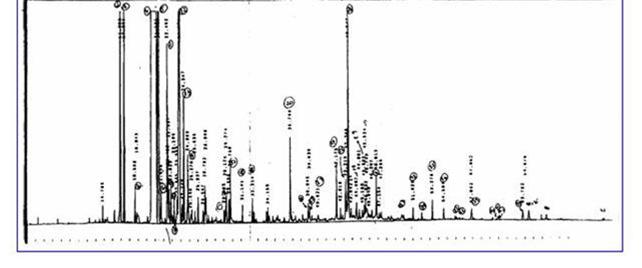
Los compuestos identificados se presentan en la Tabla 1 y los cromatogramas en la Figura 1.
Por CG y CG/MS se identificaron 17 compuestos, 8 no habían sido mencionados con anterioridad en esta especie. Estos representan el 91 % del aceite esencial, correspondiendo el 3,2% a hidrocarburos monoterpénicos, el 85% a monoterpenos oxigenados, el 0,7% a hidrocarburos sesquiterpénicos y el 2,1% a sesquiterpenos oxigenados.
Los resultados obtenidos muestran como principales componentes a la a-tujona (67.6%) y �-tujona (7.6%), coincidentes con los publicados para otras especies de Artemisia (9,10).
Se observa un alto contenido en compuestos oxigenados.
AGRADECIMIENTOS
Agradecemos al Sr. G. Schiuma por la provisión del material vegetal, y a la Dra. M. Nájera de la Universidad Nacional de La Plata por haberlo clasificado.
1 |
5 |
p-Cimeno |
2,9 |
GC/MS, IR1, IR2 |
2 |
3 |
1,8 Cineol |
2,4 |
GC/MS, IR1, IR2 |
3 |
4 |
y-Terpineno |
0,2 |
GC/MS, IR1, IR2 |
4 |
8 |
a-Tuyona |
67,6 |
GC/MS, IR1, IR2 |
5 |
9 |
�-Tuyona |
7,6 |
GC/MS, IR1, IR2 |
7 |
11 |
Alcanfor |
1,0 |
GC/MS, IR1, IR2 |
8 |
- |
cis-Pinocarveol |
0,2 |
GC/MS, IR1 |
11 |
13 |
Pinocarvona |
0,2 |
GC/MS, IR1, IR2 |
12 |
23 |
Borneol |
4,8 |
GC/MS, IR1, IR2 |
13 |
16 |
Terpinel-4-ol |
0,8 |
GC/MS, IR1, IR2 |
14 |
20 |
a-Terpineol |
0,1 |
GC/MS, IR1, IR2 |
15 |
22 |
Acetato de bornilo |
0,3 |
GC/MS, IR1, IR2 |
20 |
15 |
cis-Cariofileno |
0,5 |
GC/MS, IR1, IR2 |
- |
24 |
Carvona |
0,1 |
GC/MS, IR2 |
- |
26 |
ar-Curcumeno |
0,2 |
GC/MS, IR2 |
26 |
29 |
Epoxiisocariofileno |
1,9 |
GC/MS, IR1, IR2 |
30 |
- |
T-Cadinol |
0,2 |
GC/MS, IR1 |
* Valores expresados como porcentaje de área relativa
IR1: Índices de retención en CW-20M
IR2: Índices de retención en SE-30
|
|
|