
TRABAJOS CIENTIFICOS
Plantas medicinales, aromáticas y tintóreas.
 |
|
||
Anales de SAIPA - Sociedad Argentina para la Investigación de Productos Aromáticos
JORNADAS NACIONALES DE ACTUALIZACIÓN SOBRE RECURSOS AROMÁTICOS Y MEDICINALES
Volumen IX - NECOCHEA, 1984 - pág 22 a 25.
SUMMARY
The essential oíl of Matricaria chamomilla, was obtained by cohobation method. The yield, composición and discussion, are indicated in this communication.
La especie vegetal Matricaria chamomilla L. (Chamomilla germánica), es una hierba anual oriunda de Europa, perteneciente a la familia de las Compuestas. Su cultivo se ha extendido en la provincia de Buenos Aires, como consecuencia de que no sólo satisface las demandas internas sino que también, en los últimos años ha encontrado un favorable requerimiento en el mercado externo.
La importancia del aceite esencial se debe a que sus componentes le aportan propiedades fungicidas y bactericidas. Además cabe destacar que el chamazuleno es la materia activa del aceite de chamomilla otorgándole a éste propiedades antinflamatorias y antiespas-módicas.
En el presente trabajo estudiamos dos aceites esenciales de la especie Matricaria chamomilla L. El que llamaremos "aceite esencial de Matricaria chamomilla B", provenía del material seco aportado por una herboristería de la ciudad de Rosario; mientras que el "aceite esencial de Matricaria chamomilla A", de material adquirido a la Compañía Natuflora de la firma Jóviero S.R.L. (Buenos Aires), y la intercesión de SAIPA, a quienes agradecemos.
En ambos casos el material vegetal se encontraba compuesto de hojas, tallitos y flores secas, los que se sometieron a una destilación por arrastre con vapor (método de cohobacián), obteniéndose un rendimiento de 0,13 mi de aceite esencial por 100 gr de material vegetal para el caso de la Matricaria chamomilla B y de 0,24 mi de aceite esencial por 100 gr de material vegetal para el caso de Matricaria chamomilla A. La diferencia entre ambos rendimientos puede ser atribuida a la pérdida del aceite esencial contenido en el vegetal por un almacenamiento prolongado.
En ambos casos el líquido presentaba coloración azulada y al enfriarse tomaba una consistencia viscosa.
IDENTIFICACIÓN Y COMPOSICIÓN
Los componentes de ambos aceites esenciales fueron analizados por CGL y EM.
Condiciones operacionales del sistema acoplado CGL-EP1: columna o. V. 17; caudal de He: 25 ml/min; temperatura del inyector 200 °C; temperatura del detector 250 °C.
En la tabla I se indican los componentes identificados en los aceites A y B.
Se presentan los espectros de masa de los compuestos X, XII, XIII, comparados con los patrones guardados en la memoria magnética, los que resultaron ser:
| X | C10H16, 1 ,5-dimetil-6-metileno, espiro [ 2 ,4 ] heptano |
| XII | 1,4,9,9-tetrametil-octahidro, lH,3a,7-metanoazuleno |
| XIII | óxido de bisabolol |
De acuerdo a los resultados obtenidos se puede observar un bajo predominio en compuestos monoterpénicos, lo que puede ser atribuido a la pérdida de dichos componentes por un almacenamiento prolongado, ;o" un alto contenido en sesquiterpenoides predominantemente farneseno 'IX) y óxido de bisabolol (XIII), lo que coincidiría con Ips datos bibliográficos (4).
TABLA I
% |
% |
||||
Mirceno |
(I) |
0,26 |
- |
CGL |
- |
1,8 Cineol |
(II) |
0,57 |
- |
CGL |
- |
Linalol |
(III) |
0,08 |
- |
CGL |
- |
α Terpineol |
(IV) |
0,31 |
- |
Masa/CGL |
(1) |
Borneol |
(V) |
0,20 |
- |
CGL |
- |
Pulegona |
(VI) |
1,01 |
0,316 |
Masa/CGL |
(2) |
Chamazuleno |
(VII) |
1,05 |
0,482 |
CGL |
- |
Cariofileno |
(VIII) |
1,06 |
0,365 |
CGL |
- |
Farneseno |
(IX) |
15,42 |
10,121 |
Masa/CGL |
(2 y 3) |
C10H16 (a) |
(X) |
1,22 |
- |
Masa/CGL |
(2) |
Nerolidol |
(XI) |
1,93 |
0,871 |
CGL |
- |
C15H26 |
(XII) |
3,32 |
9,458 |
Masa/CGL |
(2) |
Oxido de bisabolol |
(XIII) |
46,11 |
52,492 |
Masa/CGL |
(2) |
Farnesol |
(XIV) |
1,93 |
2,50 |
Masa/CGL |
(2) |
Aislación y caracterización del farneseno (IX)
El farneseno fue aislado a partir del aceite esencial de Matricaria chamomilla, utilizando un cromatógrafo de gases preparativo.
Condiciones operacionales: Columna Carbowax 20 M; Temperaturas: inyector 202,7 °C, columna 191,3 °C (isotérmica), detector 215,1 °C ; caudal de gas: N2 (1 kg/cm2).
Se aisló un componente que presentaba coloración amarilla con una pureza del 80 %, el espectro RMN, coincidía con el del trans β - farneseno (5). 1,59 (6H,s); 1,65 (3H,s), 2 y 2 ,2 (8H); 4,9; 5,20 y 5,35 (6H); 6,35 (1H,dd,10Hz y 16Hz).
Aislación y caracterización del chamazuleno
Se aisló el chamazuleno a partir del aceite esencial por extracción con P04H3 al 85 % (6), posteriormente se purificó por CC, utilizando como absorbente Silicagel y como eluente hexano. Fue identificado como chamazuleno (VII) en base a su espectro RMN (7). Datos obtenidos del espectro RMNH1 (60MHz), utilizando como solvente CDCl3; equipo RMN: Varian 360 A. H l,33 (3H,t,j=7Hz) ; 2,60 (3H,s); 2,80 (3H,s); 2,85 (2H.multiplete); 7 (1H,múltiplete); 7,2 (1H);7,5 (1H, d.j=4Hz); 8,10 (lH,d,j = 2Hz).
AGRADECIMIENTOS: Al Ing. Roberto O. Piagentiní , por la colaboración de los espectros RMN efectuados; a la Sra. Gloria Appendino, por los cromatogramas realizados y al personal del CERIDE , por los espectros de masa.
CUADRO
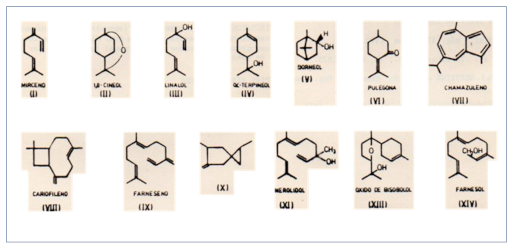
|
|
|