
TRABAJOS CIENTIFICOS
Plantas medicinales, aromáticas y tintóreas.
 |
|
||
Anales de SAIPA - Sociedad Argentina para la Investigación de Productos Aromáticos
V REUNIÓN TÉCNICA NACIONAL SOBRE ESPECIES Y PRODUCTOS AROMÁTICOS Y MEDICINALES.
Volumen VII - Castelar - 29 y 30 de Septiembre de 1982 - Páginas 47 a 57.
* Farmaceutica-Bioquímica. Trabajo realizado para la firma CHEMI S. R.L. División Química.
INTRODUCCIÓN
Se inició el trabajo efectuando una exhaustiva búsqueda bibliográfica y se contó, cuando fue necesario, con la traducción al castellano de los trabajos científicos publicados hasta el presente sobre esta especie vegetal.
De esta manera se ha podido tener una idea exacta del origen y desarrollo de las investigaciones que se llevaron a cabo en distintos países y en diferentes épocas, tendientes todas ellas a esclarecer la estructura química, las propiedades y características de los glucósidos que se encuentran en esta planta.
En el gráfico N� 1 se compara el poder edulcorante del steviósi-do y de otros sustitutos del azúcar en relación a la sacarosa.
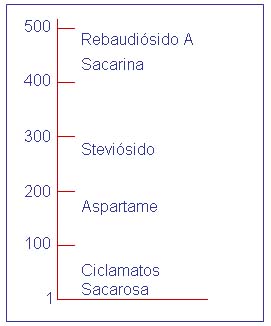
El poder edulcorante relativo de una sustancia se establece según el grado de dulcificación, determinando cuantos gramos de azúcar hay que disolver en un determinado volumen de agua para obtener el mismo sabor dulce que con un gramo de la sustancia en ensayo, en igual cantidad de mililitros de agua. El panel de prueba debe componerse de por lo menos 20-30 personas.
El Rebaudiósido A es aproximadamente 450 veces más dulce que el azúcar y se halla junto al steviósido en la hoja de Stevia rebaudiana pero en menor proporción.
Tienen una estructura química muy parecida, diferenciándose en el número de moles de glucosa unidos al aglucón, denominado Steviol.
Las fórmulas desarrolladas de los mismos se indican en la figura 1.
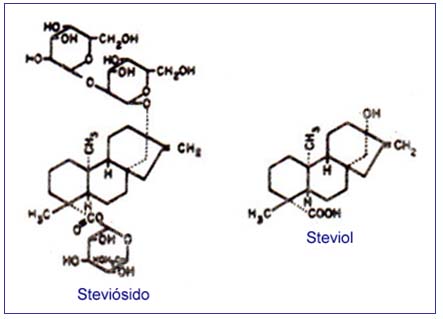
Se ha demostrado que es posible transformar el Steviósido en Rebaudiósido A (13).
El Steviol, que estructuralmente es idéntico al ácido 13-hidroxi-Kaurenoico, es insaboro pero de interés desde el punto de vista fitofisiológico, se comprobó que posee una actividad biológica del tipo de la gibberellina (hormona vegetal) (5).
Otros glucósidos han sido aislados e identificados (12-14); se hallan en muy pequeña cantidad y su poder edulcorante relativo es menor que el del Steviósido.
Las primeras comunicaciones científicas que aparecen en la literatura se remontan a 1899-1905 (1-2), cuando el Dr. Bertoni en Paraguay clasifica botánicamente esta especie, sólo conocida hasta entonces por los indígenas de la zona.
En 1899 (1) la denomina Eupatoriun rebaudianum y posteriormente (2) la clasifica Stevia rebaudiana, en honor al investigador paraguayo Dr. Rebaudi, que según palabras textuales del Dr. Bertoni: "se ocupa siempre y con tanto interés del estudio de los productos naturales de su país".
Es el Dr. Rebaudi el que publica en 1900, en la Revista de Química y Farmacia de Buenos Aires el primer análisis químico del principio dulce extraído de esta planta.
Esta especie que pertenece a la Familia de las Compuestas, tribu Asteraceae género Stevia, crece en forma silvestre en el norte del Paraguay, en el Brasil y también en el norte de nuestro país.
En Paraguay la conocían los lugareños desde tiempos remotos; ello está documentado en los informes que enviaban los conquistadores a España y se conservan en el Archivo Nacional de Asunción del Paraguay.
En guaraní se denomina "Kaá-hé-é", que significa "yerba dulce". Se empleaba para edulcorar el mate cocido, bebidas medicamentosas y en los tratamientos para personas diabéticas.
Es una planta herbácea de 30-40 cm de altura. Las hojas ovaladas un poco alargadas, con los bordes ligeramente dentados, cortamente pecioladas, casi sésiles.
El color es verde intenso en la faz inferior, siendo en la superior de color verde azulado y de aspecto lustroso.
Las hojas terminales se encuentran comunmente en grupos de tres hasta cuatro. Las flores son terminales, blancas, pequeñas.
La raíz es pivotante y mide generalmente un cuarto de la altura de la planta, la cubre una corteza fina de color débilmente terroso (24).
MATERIALES Y MÉTODOS
Este trabajo se realizó con la planta seca, proveniente de Paraguay. Se efectuó la identificación botánica y una muestra representativa se halla archivada en el Instituto Nacional de Farmacología y Bromatología - Farmacobotánica.
Los pasos seguidos para la extracción y purificación fueron los siguientes:
Técnica:
Se pesaron 200 g de polvo grueso de hojas y se extrajeron en un Soxhlet con una mezcla en partes iguales de cloroformo : éter de petróleo (40� - 60� C) durante aproximadamente 10 horas.
El polvo de hojas desengrasado se seco al vacío para eliminar los restos de solvente y se colocó nuevamente en el extractor. Se usó una mezcla de alcohol de 95� y agua destilada en c.s. para obtener un alcohol de 60�. Se extrajo aproximadamente 48 horas.
El líquido extractivo de fuerte color verde oscuro y sabor dulce se concentró al vacío, con suave calentamiento.
Se obtiene un líquido siruposo. Se toma con agua hasta obtener una solución acuosa al 20 %.
Esta solución se pasa por una columna de Amberlita I.R.-120(H). A continuación por otra columna suavemente aniónica del tipo Duolite A-4. Las columnas empleadas miden 45 mm x 800 mm. Se repitió el pasaje por ambas columnas.
Se obtiene un líquido amarillento que se concentró al vacío, en baño, de agua a 40� - 50� C.
Se obtuvo un residuo siruposo parecido a la miel, que se decoloró tratándolo con carbón activado en metanol absoluto.
La solución metanólica se deja en la heladera toda la noche y precipita un polvo blanco.
Se filtra, seca y pesa : 20,2 gramos. Recristaliza de dioxano-metanol. Seco pesa: 14 g.
P.F. : 198�-201� C.
Rendimiento obtenido: 7 %.
Identificación por cromatografía en capa delgada.
Se utilizaron placas de vidrio de 20 cm x 20 cm, recubiertas de Silicagel G, 250 micrones. Secadas al aire y luego en estufa a 105� C, 30 min. Se usó la siguiente mezcla de solventes para saturar la cámara y efectuar la corrida: butanol : metanol : agua (8:1:1).
- Solución testigo: steviosido puro al 2 % en etanol.
- Solución ensayo: steviosido obtenido al 2 % en etanol.
Se siembran 25 mc1 de cada una de las soluciones.
Revelado: cámara de iodo.
Procedimiento: a 2 cm del borde inferior de la placa, se sembraron las soluciones en estudio. Se colocó la placa en la cámara, previamente saturada con la mezcla de solventes.
Se dejó correr hasta que el frente del solvente alcanzo 15 cm aproximadamente. Se retiró la placa y se secó a temperatura ambiente. El revelado permitió visualizar dos manchas de aspecto similar en tamaño y semejante Rf = 0,56.
Se emplearon otros sistemas de solventes en forma alternativa y se obtuvieron los siguientes valores de Rf:
Método de valoración:
El steviósido en presencia del reactivo timol:sulfúrico desarrolla color que puede determinarse a 490 nm.
Este no es un método específico, pero permite determinar en forma rápida el tenor de glucósido presente en el producto obtenido.
La determinación cuantitativa del steviósido y el rebaudiósido A puede efectuarse mediante cromatografía líquida de alta perfomance (C.L.A.P.) según lo indican Hashimoto, Y. y. col. (10).
Propiedades y características del Steviósido:
El steviósido es un glucósido diterpénico, que se presenta como un polvo blanco, algo higroscópico, con un P.F. 198�-201� C.
Soluble 0,10-0,12% en agua.
Es estable en medio ácido. Así lo comprobaron Fujita H. y col. (7) al disolver el steviósido en diferentes soluciones buffer, con un plí comprendido entre 2 y 10. Al calentar en baño de agua durante una hora obtienen los resultados que se indican en la tabla I.
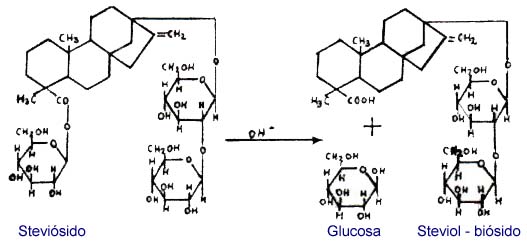
La estabilidad en medio ácido es una propiedad que facilita su empleo en bebidas gaseosas caracterizadas por su tenor ácido. En medio alcalino se elimina una molécula de glucosa y se obtiene el steviol-biósido, que posee un menor poder edulcorante que el steviósido; en la fig. N� 2 se indica el proceso mencionado.
Tabla I - ESTABILIDAD DEL STEVIÓSIDO (7)
% |
|
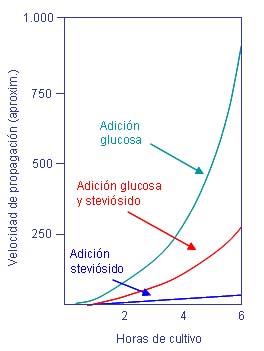
El steviósido no fermenta, lo cual representa una ventaja adicional para su uso en jarabes y bebidas (30).
Los microorganismos, agentes responsables de las caries dentales, prácticamente no se desarrollan en un medio de cultivo al cual se adiciona steviósido (gráfico N� 2) (7).
Se recomienda su uso en caramelos y en gomas de mascar en reemplazo del azúcar.
Dada la ínfima incidencia desde el punto de vista calórico puede definirse como ur edulcorante no calórico e incluirse en los regímenes hipocalóricos. Es por lo tanto apto para los pacientes que por razones metabolicas no deben ingerir azúcar.
Según el Prof. N.R. Farnsworth el Steviósido no ha demostrado ser tóxico ni tener ninguna otra actividad farmacológica, en el hombre o en los animales, de acuerdo con los diferentes trabajos de la literatura científica (6).
Hasta ahora no se ha ratificado su posible actividad anticonceptiva (22).
Investigaciones publicadas en los últimos años indican que este glucósido ha demostrado no ser riesgoso en ninguna concentración cuando se lo administra por vía oral (8-21-31).
En un trabajo se describe su actividad hipoglucemiante en conejos (26).
RESULTADOS
Mediante la puesta a punto de la técnica brevemente descripta, se obtuvo cantidad suficiente de Steviósido para elaborar una partida piloto de comprimidos.
Se efectuó la identificación del glucósido por cromatografía en capa delgada y la valoración por colorimetría.
Se dosificó la cantidad de steviósido por comprimido teniendo en cuenta el poder edulcorante relativo, seleccionando los excipientes más convenientes que facilitaran su disolución en bebidas frías y calientes.
DISCUSIÓN
El método expuesto permite en forma sencilla obtener un buen rendimiento de steviósido y deberán a partir de esa experiencia, hacerse los correspondientes ajustes para su translado a planta piloto y posterior producción industrial.
La extracción y purificación del principio edulcorante por razones económicas deberá efectuarse en un lugar próximo a la zona de cultivo.
En relación al cultivo y sus características, varios trabajos publicados describen las condiciones y los resultados obtenidos (9-18).
En 1970 se introdujeron en el Japón las primeras plantas de Stevia y en la actualidad doce compañías comercializan el producto que se extrae de sus hojas.
Se cultiva con fines comerciales en Brasil, Taiwán, Corea del Sur, Paraguay. Actualmente se cultiva con ese fin también en nuestro país. Existen plantaciones en la zona de El Soberbio, Misiones.
El INTI (Instituto Nacional de Tecnología Industrial) en una de sus secciones se dedica al desarrollo de este compuesto.
Por todo lo expuesto se considera que una labor conjunta y coordinada de productores, industriales, organismos oficiales y profesionales interesados en el desarrollo y aplicaciones de esta planta favorecerá e impulsará el empleo de la misma.
Agradecimientos:
Al Dr. J.L. Amorín (I.N.F. y B.), al Sr. H. Alvarez de la firma CHEMI y a la colaboración de las Sras. A. M. Cavagnaro y A. López.
|
|
|